Keine Artikel in Ihrem Warenkorb
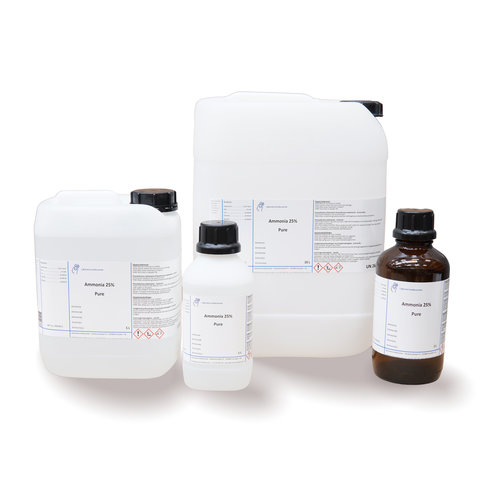
Ammoniak 25%, rein
- Kaufen Sie 2 und sparen Sie 5%
- Kaufen Sie 6 und sparen Sie 10%
Was ist Ammoniak?
Ammoniak oder Ammoniak in Wasser gelöst. ist eine chemische Verbindung von Stickstoff und Wasserstoff mit der Summenformel NH3. Es ist ein farbloses, wasserlösliches und giftiges Gas mit einem starken stechenden Geruch, der Tränen verursacht und erstickt. Ammoniak ist eine amphotere Substanz: Es wirkt unter wässrigen Bedingungen als Base. Es bildet verschiedene Reihen von Salzen: Sowohl die kationischen Ammoniumsalze als auch die anionischen Amide, Imide und Nitride, bei denen ein (Amid), zwei (Imide) oder alle (Nitride) Protonen (Wasserstoffionen) durch Metallionen ersetzt wurden.
Ammoniak ist eine der am weitesten verbreiteten Chemikalien und ein Grundmaterial für die Herstellung aller anderen Stickstoffverbindungen. Das meiste Ammoniak wird zu Düngemitteln verarbeitet, insbesondere zu Harnstoff- und Ammoniumsalzen. Bisher (2020) wurde es fast ausschließlich nach dem Haber-Bosch-Verfahren aus den Elementen Wasserstoff und Stickstoff hergestellt.
Biologisch gesehen spielt Ammoniak eine wichtige Funktion als Zwischenprodukt bei der Bildung und dem Abbau von Aminosäuren. Aufgrund der Toxizität größerer Mengen Ammoniak wird es zur Ausscheidung im Körper in ungiftigen Harnstoff oder beispielsweise bei Vögeln in Harnsäure umgewandelt.
Anwendungen
-Grundmaterial für die Herstellung aller anderen industriell hergestellten stickstoffhaltigen Verbindungen
Mit einem Anteil von 40% im Jahr 1995 ist Harnstoff die Hauptverbindung aus Ammoniak, das hauptsächlich als Dünger und zur Herstellung von Harnstoffharzen verwendet wird. Harnstoff wird durch Umsetzung von Ammoniak mit Kohlendioxid erhalten.
Neben Harnstoff werden auch andere stickstoffhaltige Düngemittel aus Ammoniak hergestellt. Am wichtigsten sind die Ammoniumsalze Ammoniumnitrat, Phosphat und Sulfat. Insgesamt betrug der Anteil der Düngemittel am gesamten Ammoniakverbrauch im Jahr 2003 83%.
Eine weitere wichtige Substanz aus Ammoniak ist Salpetersäure, die wiederum der Rohstoff für viele andere Verbindungen ist. Beim Ostwald-Verfahren reagiert Ammoniak mit Sauerstoff auf Platinnetzen unter Bildung von Stickoxiden, die mit Wasser unter Bildung von Salpetersäure reagieren.
-Rolle in verschiedenen organischen Synthesen
Primäre Carbonsäureamide können aus Ammoniak und geeigneten Carbonsäurederivaten wie Carbonsäurechloriden oder -estern erhalten werden. Im Gegensatz dazu tritt die direkte Reaktion von Carbonsäure und Ammoniak unter Bildung des entsprechenden Amids nur bei erhöhten Temperaturen auf, wenn sich das zuvor gebildete Ammoniumsalz zersetzt. Eine technisch wichtige Reaktion ist die von Adipinsäure und Ammoniak unter Bildung von Adipindinitril. Dieses wird weiter zu Hexamethylendiamin hydriert, was es zu einem Zwischenprodukt für die Nylonherstellung macht.
Es ist möglich, Anilin durch Reaktion von Phenol und Ammoniak an einem Aluminiumsilikatkatalysator herzustellen. Dieser Syntheseweg erfordert jedoch mehr Energie und hat eine geringere Ausbeute als die Synthese und Reduktion von Nitrobenzol und wird daher nur in begrenztem Umfang verwendet, wenn Phenol billig verfügbar ist.
-Spezielle Anwendungen
Die Reaktion von Ammoniak mit Säuren wird bei der Rauchgasreinigung eingesetzt. Es kann mit Schwefelsäure und Salpetersäure reagieren und entfernt so unerwünschte, umweltschädliche Schwefel- und Stickoxide aus dem Rauchgas.
Ammoniak wird aufgrund seiner hohen spezifischen Verdampfungsenthalpie von 1368 kJ / kg auch als Kältemittel eingesetzt. Vorteile sind eine geringe Entflammbarkeit, ein nicht vorhandener Beitrag zum Treibhauseffekt oder zur Zerstörung der Ozonschicht und der Anwendungsbereich von –60 bis +100 ° C. Die Toxizität der Verbindung ist nachteilig.
Ammoniaklösung wird auch in Geruchsampullen verwendet. Der extreme Geruchsreiz dient als antidissoziative Strategie, beispielsweise im Rahmen der dialektischen Verhaltenstherapie.
Ammoniak reagiert mit der im Holz enthaltenen Gerbsäure und färbt das Holz je nach Konzentration der Gerbsäure dunkelbraun. Eichenholz wird beispielsweise mit Ammoniak oder Sal-Ammoniak in dunkelbraune Räuchereiche umgewandelt. Ammoniak wird auch zum Färben bei der Herstellung von Blaupausen (Diazotypen) verwendet.
Es gibt auch experimentelle Brennstoffzellensysteme, in denen der notwendige Wasserstoff erhalten wird, wenn er durch Aufspalten des Ammoniaks unter Verwendung chemischer Verfahren benötigt wird. Ein weiterer Ansatz, der untersucht wurde, ist die Verwendung von Ammoniak als einfach zu handhabendes chemisches Energiespeichergerät, um beispielsweise überschüssigen Strom aus schwankenden erneuerbaren Energiequellen (Wind und Sonne) langfristig und industriell zu speichern Schließen Sie Lücken in der Versorgung mit diesen Energien und nutzen Sie erneuerbare Energiequellen für den Fahrzeugantrieb, beispielsweise in Schiffsmotoren. Aufgrund des Wirkungsgrades von ca. 55-60% bei der Umwandlung elektrischer Energie in chemische Energie aus Ammoniak und zurück in großen Diesel
Ammoniak kaufen?
Labor-Discounter verkauft Ammoniak in verschiedenen Verpackungen und zu einem günstigen Preis! So bestellen Sie Ihr Ammoniak schnell und einfach über Laboratoriumdiscounter.nl. Schnell versendet!
Technische Daten:
Molare Masse (M) 17,03 + aq g/mol
Dichte (D) 0,91
Siedepunkt (Kp) 37,7 °C
Schmelzpunkt (F) -57,5 °C
ADR 8 III • WGK 2
CAS-Nr. [1336-21-6]
EG-Nr. 215-647-6 • UN-Nr. 2672
Downloads
$$$$$
Gefahrenhinweise
H290 Kann für Metalle ätzend sein
H314 Verursacht schwere Verbrennungen und Augenschäden
H335 Kann Atemwegsreizungen verursachen
H400 Sehr giftig für Wasserlebewesen
Sicherheitsempfehlungen
Vorsichtsmaßnahmen - Prävention
P273 Vermeiden Sie die Freisetzung in die Umwelt.
P280 Schutzhandschuhe / Schutzkleidung / Augenschutz / Gesichtsschutz tragen.
Vorsichtsmaßnahmen - Reaktion
P303 + P361 + P353 WENN AUF DER HAUT (oder den Haaren): Kleidung sofort kontaminieren
Herausziehen. Spülen Sie die Haut mit Wasser [oder Dusche].
P305 + P351 + P338 WENN IN AUGEN: Langsam mit Wasser abspülen
Anzahl der Minuten; Kontaktlinsen nach Möglichkeit entfernen; weiter spülen.
P310 Rufen Sie sofort ein GIFTZENTRUM / einen Arzt an.