Keine Artikel in Ihrem Warenkorb
Sulfaminsäure
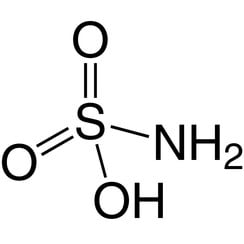
Sulfaminsäure, auch Amidosulfonsäure genannt, ist eine molekulare Verbindung mit der Formel H3NSO3. Diese farblose, wasserlösliche Verbindung findet viele Anwendungen. Sulfaminsäure schmilzt bei 205 ° C und zersetzt sich bei höheren Temperaturen zu Wasser, Schwefeltrioxid, Schwefeldioxid und Stickstoff.
Sulfaminsäure (H3NSO3) kann als Zwischenverbindung zwischen Schwefelsäure (H2SO4) und Sulfamid (H4N2SO2) angesehen werden, wobei bei jedem Schritt eine Hydroxylgruppe (-OH) durch eine Amingruppe (-NH2) ersetzt wird. Dieses Muster kann sich nicht in beide Richtungen erstrecken, ohne den Sulfonyl (-SO2–) -Rest abzubauen. Sulfamate sind Derivate der Sulfaminsäure.
Anwendungen
Sulfaminsäure ist in erster Linie eine Vorstufe für süß schmeckende Verbindungen. Die Reaktion mit Cyclohexylamin, gefolgt von der Zugabe von NaOH, ergibt C6H11NHSO3Na, Natriumcyclamat. Verwandte Verbindungen sind auch Süßstoffe wie Acesulfam-k.
Sulfamate wurden bei der Entwicklung vieler Arten von Therapeutika verwendet, wie Antibiotika, Nukleosid / Nukleotid-Human-Immundefizienz-Virus (HIV) -Reverse-Transkriptase-Inhibitoren, HIV-Protease-Inhibitoren (PIs), Krebsmedikamente (Steroidsulfatase- und Carboanhydrase-Inhibitoren), Antiepileptika und Medikamente zur Gewichtsreduktion.
-Reinigungsmittel
Sulfaminsäure wird als saures Reinigungsmittel verwendet, manchmal rein oder als Teil von proprietären Gemischen, üblicherweise für Metalle und Keramiken. Es wird oft verwendet, um Rost und Zunder zu entfernen und die flüchtigere und reizendere Salzsäure zu ersetzen, die billiger ist. Es ist häufig Bestandteil von Entkalkungsmitteln für den Haushalt, z. B. enthält Kalk-A-Way-Dickgel bis zu 8% Sulfaminsäure mit einem pH-Wert von 2,0 bis 2,2 oder Reinigungsmittel zur Entfernung von Kalk. Im Vergleich zu den meisten gängigen starken Mineralsäuren weist Sulfaminsäure wünschenswerte Wasserentkalkungseigenschaften, geringe Flüchtigkeit und geringe Toxizität auf. Es bildet wasserlösliche Salze von Kalzium und Eisen.
Aufgrund seiner Eigensicherheit ist Sulfaminsäure Salzsäure vorzuziehen. Wenn es nicht ordnungsgemäß mit Produkten auf Hypochloritbasis wie Bleichmittel gemischt wird, bildet es kein Chlorgas, während die häufigsten Säuren dies tun würden. Die Reaktion (Neutralisation) mit Ammoniak ergibt ein Salz.
Es findet auch Anwendung in der industriellen Reinigung von Milch- und Brauereimaschinen. Obwohl sie als weniger ätzend als Salzsäure angesehen werden, werden den handelsüblichen Reinigungsmitteln, deren Bestandteil sie sind, häufig Korrosionsinhibitoren zugesetzt. Es kann zum Entkalken von Kaffee- und Espressomaschinen sowie Zahnreinigern verwendet werden.
-Andere Verwendungen
- Katalysator für den Veresterungsprozess
- Herstellung von Farbstoffen und Pigmenten
- Herbizid
- Koagulator für Harnstoff-Formaldehyd-Harze
- Zutat in Feuerlöschern. Sulfaminsäure ist der Hauptrohstoff für Ammoniumsulfamat, ein weit verbreitetes Herbizid und feuerhemmendes Material für
- Haushaltsprodukte.
- Zellstoff- und Papierindustrie als Stabilisator von Chlorid
- Die deprotonierte Form (Sulfamat) ist ein übliches Gegenion für Nickel (II) beim Galvanisieren.
- Wird verwendet, um Nitritionen aus einem Gemisch aus Nitrit- und Nitrationen (NO3− + NO2−) während der qualitativen Analyse von Nitrat unter Verwendung eines Brown-Ring-Tests abzutrennen.
-Silberpolieren
Das flüssige Silberreinigungsprodukt TarnX enthält laut Etikett auf dem Verbraucherprodukt Thioharnstoff, ein Waschmittel und Sulfaminsäure.