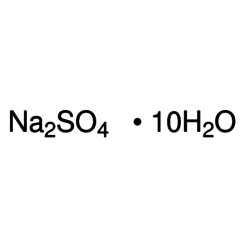No tiene ningún artículo en su cesta
Sulfato de sodio
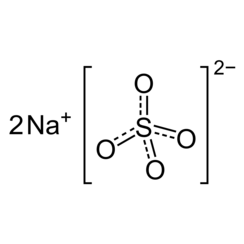
El sulfato de sodio (también conocido como sulfato de sodio o sulfato de sodio) es el compuesto inorgánico con fórmula Na2SO4 y varios hidratos relacionados. Todas las formas son sólidos blancos que son altamente solubles en agua. Con una producción anual de 6 millones de toneladas, el decahidrato es un importante producto químico básico. Se utiliza principalmente en la fabricación de detergentes y en el proceso de pulpa de papel kraft.
Aplicaciones
Industrias de materias primas
Con precios estadounidenses de 30 dólares la tonelada en 1970, hasta 90 dólares la tonelada por la calidad de la torta de sal y 130 dólares por las mejores calidades, el sulfato de sodio es un material muy barato. Su mayor uso es como relleno en detergentes domésticos en polvo y consume alrededor del 50% de la producción mundial. Este uso está disminuyendo a medida que los consumidores cambian cada vez más a detergentes compactos o líquidos que no contienen sulfato de sodio.
Otro uso previamente importante del sulfato de sodio, particularmente en los Estados Unidos y Canadá, es el proceso Kraft para hacer pulpa de madera. Las sustancias orgánicas presentes en la "bebida negra" de este proceso se queman para producir calor, que es necesario para estimular la reducción del sulfato de sodio a sulfuro de sodio. Sin embargo, los avances en la eficiencia térmica del proceso de recuperación de Kraft a principios de la década de 1960 lograron una recuperación de azufre más eficiente y redujeron drásticamente la necesidad de producción de sulfato de sodio. Por lo tanto, el uso de sulfato de sodio en la industria de la pulpa de EE. UU. Y Canadá se redujo de 1.400.000 toneladas por año en 1970 a solo aprox. 150.000 toneladas en 2006.
La industria del vidrio ofrece otra aplicación importante para el sulfato de sodio, como la segunda aplicación más grande en Europa. El sulfato de sodio se utiliza como agente de clarificación para eliminar las pequeñas burbujas de aire del vidrio fundido. Permite que el vidrio fluya y evita la formación de espuma durante el refinado. La industria del vidrio en Europa consumió 110.000 toneladas anuales estables entre 1970 y 2006.
El sulfato de sodio es importante en la fabricación de textiles, especialmente en Japón, donde tiene la mayor aplicación. El sulfato de sodio ayuda a "suavizar", reduciendo las cargas negativas en las fibras para que los tintes puedan penetrar uniformemente. A diferencia del cloruro de sodio alternativo, no afecta los recipientes de acero inoxidable que se utilizan en el teñido. Esta aplicación en Japón y Estados Unidos consumió alrededor de 100.000 toneladas en 2006.
-Industria de alimentos
El sulfato de sodio se utiliza como diluyente para colorantes alimentarios. Se conoce como aditivo del número E E514.
-Almacenamiento térmico
La alta capacidad de almacenamiento de calor en el cambio de fase de sólido a líquido y la temperatura de cambio de fase favorable de 32 ° C (90 ° F) hace que este material sea particularmente adecuado para almacenar calor solar de bajo valor para su posterior liberación en aplicaciones de calefacción de espacios. En algunas aplicaciones, el material se incorpora en baldosas térmicas colocadas en el ático, mientras que en otras, la sal se incorpora a celdas rodeadas de agua calentada con energía solar. El cambio de fase puede reducir significativamente la masa de material necesaria para un almacenamiento de calor eficaz (el calor de fusión del sulfato de sodio decahidratado es 82 kJ / mol o 252 kJ / kg [23]), con la ventaja adicional de una consistencia de temperatura siempre que haya el material está disponible en la fase correcta.
Para aplicaciones de refrigeración, una mezcla con sal común de cloruro de sodio (NaCl) reduce el punto de fusión a 18 ° C (64 ° F). El calor de fusión de NaCl · Na2SO4 · 10H2O aumenta ligeramente a 286 kJ / kg.
-Aplicaciones a pequeña escala
En el laboratorio, el sulfato de sodio anhidro se usa ampliamente como agente secante inerte para eliminar trazas de agua de soluciones orgánicas. Es más eficiente, pero más lento que el sulfato de magnesio comparable. Solo es eficaz por debajo de aproximadamente 30 ° C, pero se puede usar con una variedad de materiales ya que es bastante inerte químicamente. Se agrega sulfato de sodio a la solución hasta que los cristales ya no se agrupen.
La sal de Glauber, el decahidrato, se utiliza como laxante. Es eficaz para eliminar del cuerpo ciertos medicamentos como el acetaminofén, por ejemplo, después de una sobredosis.
En 1953, se propuso el sulfato de sodio para el almacenamiento de calor en sistemas de calefacción solar pasiva. Esto se beneficia de las inusuales propiedades de solubilidad y del alto calor de cristalización (78,2 kJ / mol).
Otros usos del sulfato de sodio incluyen descongelación de ventanas, producción de almidón, como aditivo en ambientadores de alfombras y como aditivo para alimentos para animales.
Al menos una empresa, Thermaltake, fabrica un tapete para enfriar una computadora portátil (iXoft Notebook Cooler) con sulfato de sodio decahidratado en una almohadilla de plástico acolchada. El material se licua y circula lentamente, igualando la temperatura del portátil y actuando como aislante.