No tiene ningún artículo en su cesta
Ácido gálico
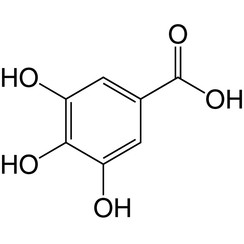
El ácido gálico (también conocido como ácido 3,4,5-trihidroxibenzoico) es un ácido trihidroxibenzoico, un tipo de ácido fenólico que se encuentra en las nueces, el zumaque, el hamamelis, las hojas de té, la corteza de roble y otras plantas. La fórmula química del ácido gálico es C6H2 (OH) 3COOH. Se encuentra solo o como parte de taninos hidrolizables. Los grupos de ácido gálico suelen estar unidos a dímeros como el ácido elágico. Los taninos hidrolizables se hidrolizan para dar ácido gálico y glucosa o ácido elágico y glucosa, conocidos como galotaninos y elagitaninos, respectivamente.
El ácido gálico forma ésteres intermoleculares (depsidos) como los ácidos digálico y trigálico, y ésteres de éter cíclicos (depsidonas).
El ácido gálico se utiliza ampliamente en la industria farmacéutica como estándar para determinar el contenido de fenol de varios analitos mediante el ensayo de Folin-Ciocalteau; los resultados se expresan en equivalentes de ácido gálico. El ácido gálico también se puede utilizar como material de partida en la síntesis del alcaloide psicodélico mescalina.
Su nombre se deriva de las agallas del roble, que tradicionalmente se utilizaban para preparar ácido tánico. A pesar del nombre, el ácido gálico no contiene galio. Las sales y ésteres del ácido gálico se denominan "galatos".
-Contexto histórico y usos
El ácido gálico es una parte importante de la tinta de galate de hierro, la tinta de escritura y dibujo estándar europea de los siglos XII al XIX, con una historia que se remonta al Imperio Romano y los Rollos del Mar Muerto. Plinio el Viejo (23-79 d.C.) describe el uso de ácido gálico como un medio para detectar un verdín falso y escribe que se usó para producir tintes. Las agallas (también llamadas manzanas de roble) de los robles se trituraron y se mezclaron con agua, creando ácido tánico. Luego se puede mezclar con vitriolo verde (sulfato ferroso) - obtenido evaporando agua saturada de sulfato de un pozo o drenaje de mina - y goma de acacia acacia; esta combinación de ingredientes produjo la tinta.
El ácido gálico fue una de las sustancias utilizadas por Angelo Mai (1782–1854), entre otros investigadores del palimpsesto, para eliminar la capa superior del texto y revelar manuscritos ocultos debajo. Mai fue la primera en usarlo, pero lo hizo "con mano dura", dejando a menudo manuscritos demasiado dañados para que otros investigadores los estudiaran posteriormente.
El ácido gálico fue estudiado por primera vez en 1786 por el químico sueco Carl Wilhelm Scheele. En 1818, el químico y farmacéutico francés Henri Braconnot (1780-1855) inventó un método más simple para purificar el ácido gálico de las agallas; El ácido gálico también fue estudiado por el químico francés Théophile-Jules Pelouze (1807–1867).
El ácido gálico es un componente de algunas mezclas de flautas pirotécnicas.
-Investigación
Es un inhibidor de la anhidrasa carbónica débil. Un estudio mostró que el ácido gálico tiene un efecto sobre la formación de proteínas amiloides al modificar las propiedades de la alfa-sinucleína, una proteína asociada con el desarrollo de enfermedades neurodegenerativas.
- Por supuesto evitar
El ácido gálico se encuentra en varias plantas terrestres, como la planta parásita Cynomorium coccineum, la planta acuática Myriophyllum spicatum y el alga verdiazul Microcystis aeruginosa. El ácido gálico también se encuentra en varias especies de robles, Caesalpinia mimosoides y en la corteza del tallo de Boswellia dalzielii. Muchos alimentos contienen cantidades variables de ácido gálico, especialmente frutas (como fresas, uvas, plátanos), té, clavo y vinagre. El fruto de la algarroba es una rica fuente de ácido gálico (24-165 mg por 100 g).
-Producción
El ácido gálico se libera fácilmente de los galotaninos por hidrólisis ácida o alcalina. Cuando el ácido gálico se calienta con ácido sulfúrico concentrado, el rufigalol se produce por condensación. La oxidación con ácido arsénico, permanganato, persulfato o yodo produce ácido elágico, así como la reacción del galato de metilo con cloruro de hierro (III).