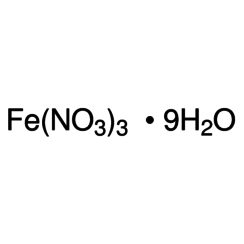No tiene ningún artículo en su cesta
Nitrato de hierro (III)
El nitrato de hierro (III) o nitrato férrico es el compuesto químico con la fórmula Fe (NO3) 3.
Propiedades químicas
Descomposición
Después de la disolución, el nitrato de hierro (III) forma una solución amarilla como resultado de la hidrólisis. Cuando se calienta hasta casi hervir, el ácido nítrico se evapora de la solución y todo el hierro se precipita como óxido de hierro (III) Fe2O3.
El compuesto se disuelve en ácido esteárico fundido y se descompone a aproximadamente 120 ° C en hidróxido de óxido de hierro (III) FeO (OH).
Preparación
El compuesto se puede preparar tratando polvo de hierro metálico con ácido nítrico.
Fe + 4 HNO3 → Fe (NO3) 3 + NO + 2 H2O.
Aplicaciones
-En el laboratorio
El nitrato de hierro (II) es el catalizador de elección para la síntesis de amida de sodio a partir de una solución de sodio en amoníaco:
2 NH3 + 2 Na → 2 NaNH2 + H2
Se ha encontrado que ciertas arcillas impregnadas con nitrato férrico son agentes oxidantes útiles en síntesis orgánica. Por ejemplo, el nitrato férrico en montmorillonita, un reactivo llamado "Clayfen", se ha utilizado para la oxidación de alcoholes a aldehídos y tioles a disulfuros.
-Otras aplicaciones
Las soluciones de nitrato de hierro son utilizadas por joyeros y herreros para grabar plata y aleaciones de plata.