Il n'y a aucun article dans votre panier
Bicarbonate de sodium
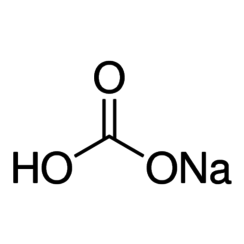
Le bicarbonate de sodium (nom IUPAC: hydrogénocarbonate de sodium), communément appelé bicarbonate de soude (en particulier en Amérique du Nord et en Nouvelle-Zélande) ou bicarbonate de sodium, est un composé chimique de formule NaHCO3. C'est un sel composé d'un cation sodium (Na +) et d'un anion bicarbonate (HCO3-). Le bicarbonate de sodium est un solide blanc cristallin, mais qui se présente souvent sous forme de poudre fine. Il a un goût légèrement salé et alcalin semblable à celui de la soude (carbonate de sodium). La forme minérale naturelle est la nahcolite. C'est un composant de la soude minérale et se trouve dissous dans de nombreuses sources minérales.
Le bicarbonate de sodium a les utilisations suivantes:
- En cuisine, le bicarbonate de soude est principalement utilisé en boulangerie comme levain. Lorsqu'il réagit avec l'acide, il libère du dioxyde de carbone, ce qui fait que la pâte se dilate et forme la texture et le grain caractéristiques des crêpes, des gâteaux, des pains rapides, du pain au soda et d'autres aliments cuits au four et frits.
Les matières acides qui provoquent cette réaction comprennent les phosphates d'hydrogène, le tartre, le jus de citron, le yogourt, le babeurre, le cacao et le vinaigre. Le bicarbonate de soude peut être utilisé avec le levain, qui est aigre, ce qui en fait un produit plus léger avec un goût moins acide.
La chaleur à elle seule peut également amener le bicarbonate de sodium à agir comme un activateur de cuisson en raison de la décomposition thermique, libérant du dioxyde de carbone à des températures supérieures à 80 ° C (180 ° F)
En utilisant cette méthode, sans la présence d'un composant acide (dans la pâte ou en utilisant une poudre à pâte contenant de l'acide), ne libèrera que la moitié du CO2 disponible (une molécule de CO2 est formée pour deux équivalents de NaHCO3 ). De plus, en l'absence d'acide, la décomposition thermique du bicarbonate de sodium produit également du carbonate de sodium, qui est hautement alcalin et donne au produit cuit un goût amer, "savonneux" et une couleur jaune. Comme la réaction est lente à température ambiante, les mélanges (pâte à gâteau, etc.) peuvent reposer sans lever jusqu'à ce qu'ils soient chauffés au four.
Lors de l'ajout d'acide, des ingrédients alcalins tels que le lait entier ou le cacao transformé aux Pays-Bas sont souvent ajoutés aux aliments cuits au four pour éviter un goût trop acide de l'acide ajouté.
La poudre à pâte, également vendue pour la cuisson, contient environ 30% de bicarbonate de soude et divers ingrédients acides qui sont activés en ajoutant de l'eau, sans qu'il soit nécessaire d'ajouter des acides supplémentaires dans le milieu de cuisson. De nombreuses formes de levure chimique contiennent du bicarbonate de sodium combiné avec du phosphate acide de calcium, du phosphate d'aluminium sodique ou du tartre. Le bicarbonate de soude est alcalin; l'acide utilisé dans la levure chimique évite un goût métallique lorsque le changement chimique pendant la cuisson provoque du carbonate de sodium
Le bicarbonate de sodium était parfois utilisé dans la cuisson des légumes verts car il confère une couleur vert vif - qui est décrite comme artificielle - car il réagit avec la chlorophylle pour produire de la chlorophylline. Cependant, cela a tendance à affecter le goût, la texture et la valeur nutritionnelle et n'est plus courant.
Le bicarbonate de soude est utilisé pour ramollir les légumineuses (pois, haricots) avant et pendant la cuisson, comme dans la recette traditionnelle britannique de pois mous pour faire tremper les pois. Le bicarbonate de sodium a pour effet principal de modifier le pH de la solution de trempage et de l'eau de cuisson; cela adoucit l'extérieur dur, raccourcit les temps de cuisson et peut changer le pourcentage de nutriments dans le plat, le goût et la consistance.
Le bicarbonate de soude peut réagir avec les acides contenus dans les aliments, y compris la vitamine C (acide L-ascorbique).
Il est utilisé dans la cuisine asiatique et latino-américaine pour attendrir la viande. Il est également utilisé dans la panure, comme pour les aliments frits, pour améliorer le croustillant et libérer les passages de vapeur afin que la chapelure ne soit pas soufflée pendant la cuisson.
-Fongicide et lutte antiparasitaire
Le bicarbonate de sodium peut être un moyen efficace de contrôler la croissance des moisissures et est enregistré comme biopesticide aux États-Unis par l'Environmental Protection Agency.
-Alcalinité / augmentation du pH
Le bicarbonate de sodium peut être ajouté aux piscines, spas et étangs de jardin pour augmenter l'alcalinité totale (augmenter le pH).
-Pyrotechnie
Le bicarbonate de sodium est l'un des principaux composants du feu d'artifice commun "serpent noir". L'effet est causé par la décomposition thermique, qui produit du dioxyde de carbone gazeux pour produire une longue cendre ressemblant à un serpent comme produit de combustion de l'autre ingrédient principal, le saccharose.
-Désinfectant doux
Il a de faibles propriétés désinfectantes et peut être un fongicide efficace contre certains organismes. Parce que le bicarbonate de soude absorbe les odeurs de moisi, il est devenu une méthode fiable pour les vendeurs de livres d'occasion pour rendre les livres moins désagréables.
-Extincteur d'incendie
Le bicarbonate de sodium peut être utilisé pour éteindre les petites graisses ou les incendies électriques en étant projeté sur le feu, car le bicarbonate de sodium libère du dioxyde de carbone lorsqu'il est chauffé. Cependant, il ne doit pas être utilisé dans les incendies de friteuses; la libération soudaine de gaz peut provoquer des éclaboussures de graisse. Le bicarbonate de sodium est utilisé dans les extincteurs à poudre chimique de la Colombie-Britannique comme alternative au phosphate de diammonium plus corrosif dans les extincteurs ABC. La nature alcaline du bicarbonate de sodium en fait le seul produit chimique sec utilisé dans les systèmes d'extinction d'incendie à grande échelle installés dans les cuisines commerciales, aux côtés de Purple-K. Parce qu'il peut agir comme un alcali, il a un léger effet de saponification sur la graisse chaude, formant une mousse savonneuse suffocante.
-Neutralisation des acides
Le bicarbonate de sodium réagit spontanément avec les acides, libérant du CO2 comme produit de réaction. Il est souvent utilisé pour neutraliser les solutions acides indésirables ou les fuites d'acide dans les laboratoires de chimie. Le bicarbonate de sodium ne convient pas pour neutraliser la base, même s'il est amphotère et réagit à la fois avec les acides et les bases.
-Utilisation médicale et santé
Le bicarbonate de sodium mélangé à de l'eau peut être utilisé comme antiacide pour traiter l'indigestion acide et les brûlures d'estomac. La réaction avec l'acide gastrique produit du sel, de l'eau et du dioxyde de carbone:
NaHCO3 + HCl → NaCl + H2O + CO2 (g)
Un mélange de bicarbonate de sodium et de polyéthylène glycol tel que PegLyte, dissous dans l'eau et pris par voie orale, est un lavage gastro-intestinal efficace et un laxatif avant une chirurgie gastro-intestinale, une gastroscopie, etc.
Le bicarbonate de sodium intraveineux en solution aqueuse est parfois utilisé pour les cas d'acidose ou lorsqu'il n'y a pas assez d'ions sodium ou bicarbonate dans le sang. En cas d'acidose respiratoire, l'ion bicarbonate infusé entraîne le tampon acide carbonique / bicarbonate du plasma vers la gauche et augmente ainsi le pH. Pour cette raison, le bicarbonate de sodium est utilisé dans la réanimation cardio-pulmonaire médicalement contrôlée. La perfusion de bicarbonate n'est indiquée que lorsque le pH sanguin est clairement bas (<7,1–7,0).
Le HCO3− est utilisé pour traiter l'hyperkaliémie car il refoulera K + dans les cellules pendant l'acidose. Étant donné que le bicarbonate de sodium peut provoquer une alcalose, il est parfois utilisé pour traiter un surdosage avec de l'aspirine. L'aspirine a besoin d'un environnement acide pour une bonne absorption, et l'environnement basique réduit l'absorption d'aspirine en cas de surdosage. Le bicarbonate de sodium a également été utilisé dans le traitement du surdosage d'antidépresseurs tricycliques. Il peut également être appliqué localement sous forme de pâte, avec trois parties de bicarbonate de soude pour une partie d'eau, pour soulager certains types de piqûres et de piqûres d'insectes (ainsi que le gonflement associé).
Certains praticiens alternatifs, tels que Tullio Simoncini, ont promu le bicarbonate de soude en tant qu'agent anticancéreux, dont l'American Cancer Society a mis en garde à la fois pour son efficacité non prouvée et le danger potentiel de son utilisation. Edzard Ernst a qualifié la promotion du bicarbonate de sodium en tant qu'agent anticancéreux de "l'une des formes alternatives les plus nauséabondes d'escroqueries contre le cancer que j'ai vues depuis longtemps".
Le bicarbonate de sodium peut être ajouté aux anesthésiques locaux pour accélérer l'apparition de leurs effets et rendre leur injection moins douloureuse. Il fait également partie de la solution de Moffett, utilisée en chirurgie nasale.
Dès les années 1920, on a découvert que le bicarbonate provoquait une augmentation de la résistance osseuse chez les patients qui perdaient du calcium dans leur urine. En 1968, on croyait que les régimes qui produisaient trop d'acide mettaient les os en danger. Des expériences menées par Anthony Sebastian de l'Université de Californie à San Francisco à la fin du 20e siècle ont montré que le corps décompose les os et les muscles pour libérer des carbonates, des phosphates et de l'ammoniac, qui neutralisent l'acide. L'ajout de bicarbonate de soude à l'alimentation (il a choisi d'utiliser le saleratus sans sodium, le bicarbonate de potassium) a réduit la perte de calcium chez les femmes ménopausées, ce qui représente l'équivalent d'un os «bras et jambe» pour deux. décennies.
Tout comme la pâtisserie, le bicarbonate de sodium est utilisé avec un acide doux tel que l'acide tartrique comme excipient dans les comprimés effervescents: lorsqu'un tel comprimé tombe dans un verre d'eau, le carbonate quitte le milieu réactionnel sous forme de gaz carbonique (HCO3− + H + → H2O + CO2 ↑ ou plus précisément, HCO3− + H3O + → 2 H2O + CO2 ↑), qui maintient le médicament dissous dans l'eau (dans cet exemple le tartrate de sodium) avec le sel résultant.
-Hygiène personnelle
Le dentifrice contenant du bicarbonate de sodium a été démontré dans plusieurs études pour avoir une meilleure fonction de blanchiment et d'élimination de la plaque dentaire que le dentifrice sans lui.
Le bicarbonate de sodium est également utilisé comme ingrédient dans certains bains de bouche. Il a des propriétés anti-caries et abrasives. Il agit comme un nettoyant mécanique sur les dents et les gencives, neutralise la production d'acide dans la bouche et agit également comme antiseptique pour aider à prévenir les infections. Le bicarbonate de sodium en combinaison avec d'autres ingrédients peut être utilisé pour fabriquer un déodorant sec ou humide. Le bicarbonate de sodium peut être utilisé comme tampon, combiné avec du sel de table, pour créer une solution d'irrigation nasale.
-Il est utilisé en hygiène oculaire pour traiter la blépharite. Cela se fait en ajoutant une cuillère à café de bicarbonate de sodium à de l'eau récemment bouillie, puis en frottant doucement la base des cils avec un coton-tige trempé dans la solution.
-Utilisation vétérinaire
Le bicarbonate de sodium est utilisé comme complément alimentaire pour les bovins, notamment comme tampon pour le rumen.
-Dans les sports
Bien que de petites doses de bicarbonate de sodium aient été utilisées comme supplément pour les athlètes lors d'événements de vitesse, tels que la course de moyenne distance, les preuves de bénéfices sont insuffisantes et le surdosage est un risque pour la santé car le bicarbonate de sodium peut provoquer une irritation gastro-intestinale.
-Agent de nettoyage
Le bicarbonate de sodium est utilisé dans un processus d'élimination de la peinture et de la corrosion appelé grenaillage à la soude; le procédé est particulièrement adapté au nettoyage des panneaux d'aluminium qui peuvent être déformés par d'autres types d'abrasifs.
Un fabricant recommande une pâte à base de bicarbonate de soude avec un minimum d'eau comme poudre à récurer douce et est utile pour éliminer la rouille de surface, car la rouille forme un composé soluble dans l'eau dans une solution alcaline concentrée; de l'eau froide doit être utilisée car les solutions d'eau chaude peuvent corroder l'acier. Le bicarbonate de sodium attaque la fine couche protectrice d'oxyde qui se forme sur l'aluminium, le rendant impropre au nettoyage de ce métal. Une solution dans de l'eau chaude éliminera les dépôts d'argent si l'argent entre en contact avec un morceau de papier d'aluminium. Le bicarbonate de soude est souvent ajouté aux machines à laver en remplacement de l'adoucisseur d'eau et pour éliminer les odeurs des vêtements. Il est également efficace pour éliminer les taches de thé et de café sur les tasses lorsqu'il est dilué avec de l'eau tiède. Le bicarbonate de soude peut également être utilisé comme un dissolvant d'odeur polyvalent.
Pendant le projet de Manhattan de développement de la bombe atomique au début des années 1940, la toxicité chimique de l'uranium était un problème. Les oxydes d'uranium semblent très bien adhérer au tissu de coton et ne sont pas rincés avec du savon ou un détergent. Cependant, l'uranium serait emporté par une solution à 2% de bicarbonate de sodium. Les vêtements peuvent être contaminés par de la poussière d'uranium appauvri (UD) toxique, qui est très dense et est donc utilisée pour les contrepoids dans un contexte civil et dans les projectiles perforants. L'UA n'est pas éliminé par un lavage normal; laver avec environ 6 onces (170 g) de bicarbonate de soude dans 2 gallons (7,5 L) d'eau aidera à le rincer.