Il n'y a aucun article dans votre panier
Pentoxyde de phosphore
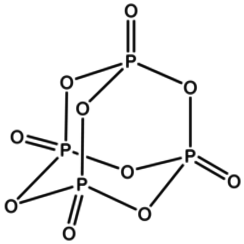
Le pentoxyde de phosphore est un composé chimique de formule moléculaire P4O10 (avec le nom commun dérivé de la formule empirique P2O5). Ce solide cristallin blanc est l'anhydride de l'acide phosphorique. C'est un puissant agent desséchant et déshydratant.
Applications
Le pentoxyde de phosphore est un puissant déshydratant comme en témoigne le caractère exothermique de l'hydrolyse:
P4O10 + 6 H2O → 4 H3PO4 (–177 kJ)
Cependant, l'utilité pour le séchage est quelque peu limitée par la tendance à former un revêtement visqueux protecteur qui empêche le séchage supplémentaire par le matériau inutilisé. Une forme granulaire de P4O10 est utilisée dans les dessiccateurs.
Conformément à son fort pouvoir desséchant, le P4O10 est utilisé en synthèse organique pour la déshydratation. Son application principale est la conversion d'amides primaires en nitriles:
P4O10 + RC (O) NH2 → P4O9 (OH) 2 + RCN
Le coproduit P4O9 (OH) 2 indiqué est une formule idéalisée pour des produits non définis en raison de l'hydratation du P4O10.
Alternativement, en combinaison avec un acide carboxylique, le résultat est l'anhydride correspondant:
P4O10 + RCO2H → P4O9 (OH) 2 + [RC (O)] 2O
Le "réactif Onodera", une solution de P4O10 dans du DMSO, est utilisé pour l'oxydation des alcools. Cette réaction rappelle l'oxydation de Swern.
La capacité de séchage du P4O10 est suffisamment forte pour convertir de nombreux acides minéraux en leurs anhydrides. Exemples: HNO3 est converti en N2O5; H2SO4 est converti en SO3; HClO4 est converti en Cl2O7; CF3SO3H est converti en (CF3) 2S2O5