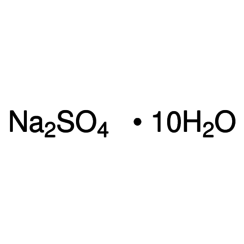Il n'y a aucun article dans votre panier
Sulfate de sodium
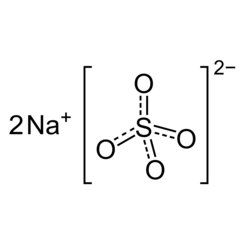
Le sulfate de sodium (également appelé sulfate de sodium ou sulfate de sodium) est le composé inorganique de formule Na2SO4 et divers hydrates associés. Toutes les formes sont des solides blancs hautement solubles dans l'eau. Avec une production annuelle de 6 millions de tonnes, le décahydrate est un produit chimique de base important. Il est principalement utilisé dans la fabrication de détergents et dans le processus kraft de pâte à papier.
Applications
Industries des matières premières
Avec des prix américains de 30 $ la tonne en 1970, jusqu'à 90 $ la tonne pour la qualité du gâteau de sel et 130 $ pour les meilleures qualités, le sulfate de sodium est un matériau très bon marché. Sa plus grande utilisation est comme charge dans les détergents ménagers en poudre et consomme environ 50% de la production mondiale. Cette utilisation est en baisse car les consommateurs se tournent de plus en plus vers des détergents compacts ou liquides qui ne contiennent pas de sulfate de sodium.
Une autre utilisation auparavant importante du sulfate de sodium, en particulier aux États-Unis et au Canada, est le procédé Kraft de fabrication de pâte de bois. Les substances organiques présentes dans la «boisson noire» de ce procédé sont brûlées pour produire de la chaleur, qui est nécessaire pour stimuler la réduction du sulfate de sodium en sulfure de sodium. Cependant, les progrès de l'efficacité thermique du procédé de récupération Kraft au début des années 1960 ont permis une récupération plus efficace du soufre et réduit considérablement le besoin de production de sulfate de sodium. Par conséquent, l'utilisation du sulfate de sodium dans l'industrie de la pâte aux États-Unis et au Canada est passée de 1 400 000 tonnes par an en 1970 à seulement env. 150 000 tonnes en 2006.
L'industrie du verre offre une autre application importante du sulfate de sodium, en tant que deuxième application en Europe. Le sulfate de sodium est utilisé comme agent de clarification pour éliminer les petites bulles d'air du verre fondu. Il permet au verre de s'écouler et empêche la formation de mousse lors du raffinage. L'industrie du verre en Europe a consommé un volume stable de 110 000 tonnes par an entre 1970 et 2006.
Le sulfate de sodium est important dans la fabrication textile, en particulier au Japon, où il est le plus utilisé. Le sulfate de sodium aide à «lisser», réduisant les charges négatives sur les fibres afin que les colorants puissent pénétrer uniformément. Contrairement au chlorure de sodium alternatif, il n'affecte pas les récipients en acier inoxydable utilisés pour la teinture. Cette application au Japon et aux États-Unis a consommé environ 100 000 tonnes en 2006.
-Industrie alimentaire
Le sulfate de sodium est utilisé comme diluant pour le colorant alimentaire. Il est connu sous le nom d'additif E514.
-Stockage thermique
La capacité de stockage de chaleur élevée lors du changement de phase du solide au liquide et la température de changement de phase favorable de 32 ° C (90 ° F) rendent ce matériau particulièrement adapté au stockage de la chaleur solaire de faible valeur pour une libération ultérieure dans les applications de chauffage des locaux. Dans certaines applications, le matériau est incorporé dans des carreaux thermiques placés dans le grenier, tandis que dans d'autres, le sel est incorporé dans des cellules entourées d'eau chauffée par le soleil. Le changement de phase peut réduire considérablement la masse de matière nécessaire à un stockage efficace de la chaleur (la chaleur de fusion du sulfate de sodium décahydraté est de 82 kJ / mol ou 252 kJ / kg [23]), avec l'avantage supplémentaire d'une consistance de la température tant qu'il y en a suffisamment le matériel est disponible dans la phase correcte.
Pour les applications de refroidissement, un mélange avec du sel de chlorure de sodium (NaCl) commun abaisse le point de fusion à 18 ° C (64 ° F). La chaleur de fusion de NaCl · Na2SO4 · 10H2O est légèrement augmentée à 286 kJ / kg.
-Applications à petite échelle
En laboratoire, le sulfate de sodium anhydre est largement utilisé comme agent de séchage inerte pour éliminer les traces d'eau des solutions organiques. Il est plus efficace, mais plus lent que le sulfate de magnésium comparable. Il n'est efficace qu'en dessous d'environ 30 ° C, mais il peut être utilisé avec une variété de matériaux car il est assez chimiquement inerte. Du sulfate de sodium est ajouté à la solution jusqu'à ce que les cristaux ne s'agglutinent plus.
Le sel de Glauber, le décahydraté, est utilisé comme laxatif. Il est efficace pour éliminer certains médicaments tels que l'acétaminophène de l'organisme, par exemple après un surdosage.
En 1953, le sulfate de sodium a été proposé pour le stockage de chaleur dans les systèmes de chauffage solaire passif. Cela profite des propriétés de solubilité inhabituelles et de la chaleur élevée de cristallisation (78,2 kJ / mol).
D'autres utilisations du sulfate de sodium comprennent la décongélation des fenêtres, la production d'amidon, comme additif dans les assainisseurs de tapis et comme additif pour l'alimentation animale.
Au moins une entreprise, Thermaltake, fabrique un tapis de refroidissement pour ordinateur portable (iXoft Notebook Cooler) avec du sulfate de sodium décahydraté dans un coussin en plastique rembourré. Le matériau se liquéfie et circule lentement, égalisant la température de l'ordinateur portable et servant d'isolation.