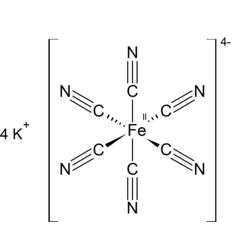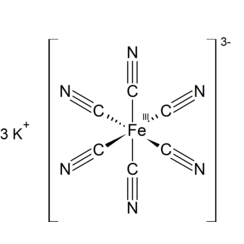Il n'y a aucun article dans votre panier
Hexacyanoferrate de potassium
Le ferricyanure de potassium, l'hexacyanoferrate de potassium ou le sel de lessive de sang rouge est le composé chimique de formule K3 [Fe (CN) 6]. Ce sel rouge vif contient l'ion [Fe (CN) 6] 3− de coordonnée octaédrique. [2] Il est soluble dans l'eau et la solution présente une certaine fluorescence vert-jaune. Il a été découvert en 1822 par Léopold Gmelin et a été initialement utilisé dans la production de colorants outremer.
Le composé est largement utilisé dans les dessins de plans et en photographie (procédé cyanotype). Le ferricyanure de potassium est utilisé dans divers tons d'impression photographique. Le ferricyanure de potassium a été utilisé comme agent oxydant pour éliminer l'argent lors du traitement des négatifs et positifs couleur, un processus appelé blanchiment. Étant donné que les agents de blanchiment au ferricyanure de potassium sont nocifs pour l'environnement, de courte durée et capables de libérer du cyanure d'hydrogène lorsqu'ils sont mélangés à de l'acide, les agents de blanchiment EDTA ferriques sont utilisés dans le traitement des couleurs depuis l'introduction du procédé Kodak C-41 en 1972. En lithographie couleur, le ferricyanure de potassium est utilisé pour réduire la taille des points de couleur sans réduire le nombre, en tant que type de correction manuelle des couleurs appelée gravure de points. Il est également utilisé en photographie noir et blanc avec du thiosulfate de sodium (hypo) pour réduire la densité d'un tirage négatif ou à la gélatine argentique, le mélange étant connu sous le nom d'agent réducteur de Farmer; cela peut aider à résoudre les problèmes causés par la surexposition du négatif ou à éclaircir les reflets de l'impression.
Le composé est également utilisé pour durcir le fer et l'acier, dans la galvanoplastie, la teinture de la laine, comme réactif de laboratoire et comme agent oxydant doux en chimie organique.
Le ferricyanure de potassium est également l'un des deux composés présents dans la solution d'indicateur de ferroxyle (avec la phénolphtaléine) qui vire au bleu (bleu de Prusse) en présence d'ions Fe2 +, et peut donc être utilisé pour détecter l'oxydation du métal qui conduira à la rouille. Il est possible de calculer le nombre de moles d'ions Fe2 + à l'aide d'un colorimètre, en raison de la couleur très intense du bleu de Prusse Fe4 [Fe (CN) 6] 3.
Le ferricyanure de potassium est souvent utilisé dans les expériences physiologiques comme moyen d'augmenter le potentiel redox d'une solution (E ° ~ 436 mV à pH 7). En tant que tel, il peut oxyder le cytochrome c réduit (E ° '~ 247 mV à pH 7) dans des mitochondries isolées intactes. Le dithionite de sodium est couramment utilisé comme agent réducteur dans de telles expériences (E ~ -420 mV à pH 7).
l'hexacyanoferrate de potassium est utilisé pour déterminer le pouvoir réducteur ferrique d'un échantillon (extrait, composé chimique, etc.). Une telle mesure est utilisée pour déterminer la propriété antioxydante d'un échantillon.
Le ferricyanure de potassium est utilisé dans de nombreux biocapteurs ampérométriques comme agent de transfert d'électrons qui remplace l'agent de transfert d'électrons naturel d'une enzyme, telle que l'oxygène, comme avec l'enzyme glucose oxydase. Il est utilisé comme cet ingrédient dans de nombreux glucomètres disponibles dans le commerce pour les diabétiques.
Le ferricyanure de potassium est combiné avec de l'hydroxyde de potassium (ou de l'hydroxyde de sodium comme substitut) et de l'eau pour formuler le décapant de Murakami. Cet agent de gravure est utilisé par les métallographes pour fournir un contraste entre les phases de liant et de carbure dans les carbures cémentés.
-BleuPruisic
Le bleu de Prusse, le pigment bleu profond du blueprint, est généré par la réaction de K3 [Fe (CN) 6] avec des ions ferreux (Fe2 +) et K4 [Fe (CN) 6] avec des sels de fer.
En histologie, le ferricyanure de potassium est utilisé pour détecter le fer ferreux dans les tissus biologiques. Le ferricyanure de potassium réagit avec le fer ferreux en solution acide pour produire le pigment bleu insoluble, communément appelé bleu Turnbull ou bleu de Prusse. Pour détecter le fer (Fe3 +) fer, le ferrocyanure de potassium est utilisé à la place de la méthode de coloration au bleu de Prusse de Perls. Le matériau formé dans la réaction au bleu de Turnbull et le composé formé dans la réaction au bleu de Prusse sont les mêmes.