Non ci sono articoli nel tuo carrello
Piridina 99,75+% extra purissimo
- Buy 2 and save 5%
- Buy 6 and save 10%
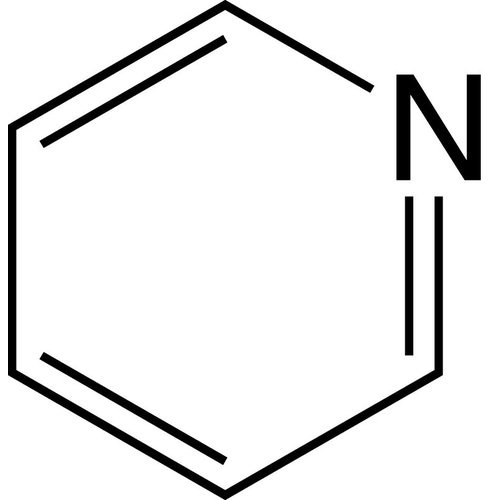
La piridina o azina, con formula chimica C5H5N, è un composto eterociclico semplice e basico che approssima la struttura del benzene, con uno dei gruppi CH sostituito da un atomo di azoto. Si presenta come un liquido limpido, leggermente giallastro, con un odore sgradevole e pungente (acido, marcio e che ricorda il pesce). È ampiamente usato nella chimica di coordinazione come ligando e in chimica organica come reagente e solvente. I derivati della piridina sono molto numerosi nei prodotti farmaceutici e agrochimici. La piridina è utilizzata come precursore nella produzione di insetticidi, erbicidi, medicinali, aromi alimentari, coloranti, adesivi, vernici e disinfettanti. È un composto aromatico che ha una reattività diversa dal benzene.
La piridina è un liquido in condizioni normali di pressione e temperatura. La piridina è miscibile con acqua e con i più comuni solventi organici. La piridina è una molecola di media polarità, meno polare dell'acqua e degli alcoli, ma più polare dell'acetato di etile, del diclorometano, dell'etere di petrolio e degli alcani. Nella NMR protonica, la piridina appare sotto tre picchi21: 8,5 ppm per l'idrogeno dell'azoto, 7,6 ppm per l'idrogeno e 7,2 ppm nel . Nell'NMR del carbonio, la piridina è ancora al di sotto di tre picchi: a 150 ppm per il carbonio 1 e 5, 139 ppm per il carbonio 3 e 123 ppm per il carbonio 2 e 421. Nella spettroscopia a infrarossi, la piridina mostra una banda di assorbimento di circa 3.000 cm−1 per il C-H dei carboni sp222. La soglia di rilevazione olfattiva è 0,02 ppm (in aria). L'indice di rifrazione è 1.51024. La costante dielettrica a 25°C è 12.425
La piridina è comunemente usata come reagente o catalizzatore nella sintesi organica in condensazione, dealogenazione, alogenazione o acilazione e anche come precursore per la sintesi di intermedi utilizzati nella produzione di insetticidi, erbicidi, prodotti farmaceutici, aromi alimentari, coloranti, adesivi, vernici, esplosivi e disinfettanti. La piridina viene quindi utilizzata come precursore di reazioni di sostituzione nucleofila e più raramente di sostituzioni elettrofile o reazioni di alchilazione sull'azoto. La piridina viene anche utilizzata per denaturare alcol, antigelo e fungicidi, e anche come coadiuvante per le tinture tessili.
La piridina è spesso usata come solvente basico polare e aiuta a neutralizzare la formazione di acido in determinate reazioni. La piridina viene spesso utilizzata come solvente polare aprotico di base o viene semplicemente aggiunta al mezzo di reazione per neutralizzare gli acidi risultanti da queste reazioni. Tuttavia, a causa dell'elevata temperatura di ebollizione, la piridina è talvolta difficile da rimuovere e vengono utilizzati altri solventi organici con una bassa temperatura di ebollizione.
La d5-piridina deuterata, in cui gli atomi di idrogeno della piridina sono stati sostituiti da atomi di deuterio, può essere utilizzata come solvente nella spettroscopia NMR.
La piridina e i suoi derivati possono essere utilizzati per attivare determinate reazioni di acilazione o esterificazione.
La 4-dimetilaminopiridina (DMAP) viene utilizzata per attivare le anidridi durante le reazioni di acilazione. L'intermedio è un sale 1-acilpiridico che reagisce con un'ammina primaria o secondaria per formare un'ammide.
La 4-(1-pirrolidinil)-piridina (PPY) attiva una reazione di esterificazione tra un acido carbossilico e alcuni alcoli in presenza di DCC (dicicloesilcarbodiimmide). Il PPY reagisce con l'intermedio formato dalla reazione tra acido e DCC, che si comporta in modo simile a un'anidride acida.
La piridina è ampiamente utilizzata come ligando nella chimica di coordinazione (in questo contesto è abbreviata in "py") perché ha una grande capacità di formare complessi con molti cationi di metalli di transizione. La piridina è un ligando abbastanza morbido nella teoria HSAB. Nei complessi si forma un legame azoto-metallo. Questi complessi possono essere utilizzati per analisi selettive.
Alcuni dei complessi piridinici sono usati per ossidare alcoli primari o secondari.
Il reagente di Collins o Sarret è costituito da un equivalente di acido cromico e due equivalenti di piridina. Si preparano per riscaldamento e si differenziano tra loro per la loro forma cristallina.
Il reagente di Conforth è costituito da un equivalente di triossido di cromo e due equivalenti di piridina mescolati con acqua
Il dicromato di piridinio PDC è costituito da un dicromato equivalente di due equivalenti di piridina e acido cloridrico
Il clorocromato di piridinio PCC è costituito da un equivalente di triossido di cromo, un equivalente di acido cloridrico e piridina.
La piridina, con acido barbiturico, viene spesso utilizzata per la rilevazione colorimetrica dei cianuri in soluzione acquosa. Reagisce con il cloruro di cianuro (formato dalla reazione tra ione cianuro e cloramina-T) per formare una specie coniugata con due molecole di acido barbiturico, che insieme hanno una tonalità rossa. L'intensità del colore è direttamente proporzionale alla concentrazione di cianuro.
Technische gegevens:
Empirical formula C5H5N
Molar mass (M) 79,10 g/mol
Density (D) 0,98
Boiling point (bp) ca. 115 °C
Flash point (flp)17 °C • Melting point (mp)-42 °C
ADR 3 II • WGK 2
CAS No.[110-86-1]
EG-Nr. 203-809-9 • UN-Nr. 1282
Downloads
$$$$$
Hazard statements
H225 Highly flammable liquid and vapor
H302 + H312 + H332 Harmful if swallowed, in contact with skin or if inhaled
H315 Causes skin irritation
H319 Causes serious eye irritation
Precautions - prevention
P210 Keep away from open flames and hot surfaces. Do not smoke.
P233 Keep container tightly closed.
P280 Wear protective gloves / eye protection.
Precautions - response
P302 + P352 IF ON SKIN: Wash with plenty of water.
P304 + P340 IF INHALED: Remove person to fresh air and keep comfortable for breathing.
P305 + P351 + P338 IF IN EYES: Rinse cautiously with water for a long period of time
amount of minutes; remove contact lenses, if possible; keep rinsing.