Non ci sono articoli nel tuo carrello
Fenolftaleina
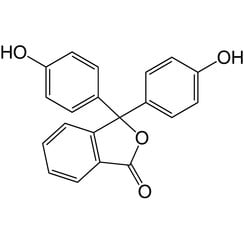
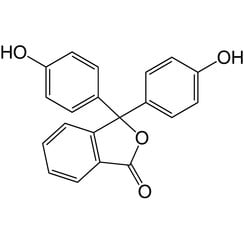
La fenolftaleina è un composto chimico con la formula C20H14O4 ed è brevemente scritto come "HIn" o "phph". La fenolftaleina è spesso utilizzata come indicatore nelle titolazioni acido-base. Per questa applicazione diventa incolore nelle soluzioni acide e rosa nelle soluzioni basiche. Appartiene alla classe dei coloranti noti come coloranti di ftaleina.
La fenolftaleina è scarsamente solubile in acqua e di solito è disciolta in alcoli per l'uso negli esperimenti. È un acido debole che può perdere ioni H + in soluzione. La molecola di fenolftaleina è incolore e lo ione fenolftaleina è rosa. Quando una base viene aggiunta alla fenolftaleina, l'equilibrio si sposta portando a una maggiore ionizzazione quando gli ioni H + vengono rimossi. Questo è previsto dal principio di Le Chatelier.
Applicazioni
Indicatore di pH
L'uso diffuso della fenolftaleina è un indicatore delle titolazioni acido-base. Serve anche come componente dell'indicatore universale, insieme al rosso di metile, al blu di bromotimolo e al blu di timolo.
La fenolftaleina assume almeno quattro diversi stati in soluzione acquosa a causa dei cambiamenti di pH. In condizioni fortemente acide esiste in forma protonata (HIn +), che gli conferisce un colore arancione. Tra condizioni fortemente acide e leggermente basiche, la forma lattonica (HIn) è incolore. La forma fenolato doppiamente deprotonato (In2) (la forma anionica del fenolo) conferisce il familiare colore rosa. In soluzioni altamente basiche, la fenolftaleina viene convertita nella sua forma In (OH) 3 e il colore rosa subisce una reazione di dissolvenza piuttosto lenta e diventa completamente incolore al di sopra di 13,0 pH.
-Carbonatazione del calcestruzzo
La sensibilità al pH della fenolftaleina viene sfruttata in altre applicazioni: il calcestruzzo ha naturalmente un pH elevato a causa dell'idrossido di calcio che si forma quando il cemento Portland reagisce con l'acqua. Quando il calcestruzzo reagisce con l'anidride carbonica nell'atmosfera, il pH scende a 8,5-9. Quando una soluzione di fenolftaleina all'1% viene applicata al calcestruzzo normale, diventa rosa brillante. Tuttavia, se rimane incolore, mostra che il calcestruzzo ha subito la carbonatazione. In un'applicazione simile, alcuni spackling usati per riparare i buchi nel muro a secco contengono fenolftaleina. Durante l'applicazione, il materiale di base della confezione mantiene un colore rosa; quando lo spackling è indurito per reazione con anidride carbonica atmosferica, il colore rosa si attenua.
-Educativo
In una soluzione molto semplice, il lento cambiamento della fenolftaleina da rosa a incolore quando convertito nella sua forma In (OH) 3 viene utilizzato nelle lezioni di chimica per lo studio della cinetica di reazione.
-Divertimento
La fenolftaleina viene utilizzata nei giocattoli, come parte dell'inchiostro che scompare o della vernice che scompare sui capelli di Hollywood Hair Barbie. Nell'inchiostro è mescolato con idrossido di sodio, che reagisce con l'anidride carbonica nell'aria. Questa reazione fa sì che il pH scenda al di sotto della soglia di cambiamento di colore quando gli ioni idrogeno vengono rilasciati dalla reazione:
OH− (aq) + CO2 (g) → CO2−
3 (aq) + H + (aq).
Per sviluppare i capelli e motivi grafici "magici", l'inchiostro viene spruzzato con una soluzione di idrossido, che porta alla comparsa delle immagini nascoste con lo stesso meccanismo sopra descritto per il cambiamento di colore in soluzione alcalina. A causa della reazione con l'anidride carbonica, il pattern alla fine scompare. La timolftaleina viene utilizzata per lo stesso scopo e allo stesso modo quando si desidera un colore blu.
-Uso medico
La fenolftaleina è stata utilizzata come lassativo per oltre un secolo, ma ora viene rimossa dai lassativi da banco a causa delle preoccupazioni sulla cancerogenicità. I prodotti lassativi che in precedenza contenevano fenolftaleina sono stati spesso riformulati con principi attivi alternativi: Feen-a-Mint è passato al bisacodile e Ex-Lax è passato a un estratto di senna.
La timolftaleina è un lassativo correlato a base di timolo.
Nonostante le preoccupazioni per la sua cancerogenicità, è improbabile che l'uso della fenolftaleina come lassativo provochi il cancro alle ovaie. È stato riscontrato che la fenolftaleina inibisce l'afflusso di calcio cellulare umano attraverso l'ingresso del calcio in negozio (SOCE, vedere Attivazione del canale di rilascio del calcio § Struttura). Ciò è ottenuto dalla trombina inibitoria e dalla thapsigargin, due attivatori di SOCE che aumentano il calcio libero intracellulare.
La fenolftaleina è stata aggiunta all'elenco dei candidati per sostanze estremamente preoccupanti (SVHC) dell'Agenzia europea per le sostanze chimiche. [14]
Una forma ridotta di fenolftaleina, la fenolftalina, che è incolore, viene utilizzata in un test per identificare le sostanze che si ritiene contengano sangue, comunemente noto come test di Kastle-Meyer. Un campione secco viene raccolto con un batuffolo di cotone o carta da filtro. Alcune gocce di alcol, poi alcune gocce di fenolftalina e infine alcune gocce di perossido di idrogeno sono gocciolate sul campione. Se il campione contiene emoglobina, diventerà immediatamente rosa dopo l'aggiunta del perossido a causa della formazione di fenolftaleina. Un test positivo indica che il campione contiene emoglobina ed è quindi probabile che sia sangue. Un falso positivo può essere dovuto alla presenza di sostanze con un'attività catalitica simile all'emoglobina. Questo test non è distruttivo per il campione; può essere salvato e utilizzato in ulteriori test. Questo test ha la stessa reazione con il sangue di qualsiasi animale il cui sangue contiene emoglobina, inclusi quasi tutti i vertebrati; sarebbero necessari ulteriori test per determinare se provenisse da un essere umano.
La fenolftaleina può essere prodotta condensando l'anidride ftalica con due equivalenti di fenolo in condizioni acide (da cui il nome). Fu scoperto nel 1871 da Adolf von Baeyer.
La reazione può anche essere catalizzata da un m