U heeft geen artikelen in uw winkelwagen
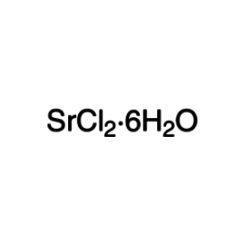
Strontiumchloride
Strontiumchloride (SrCl2) is een zout van strontium en chloor. Het is een typisch zout dat neutrale waterige oplossingen vormt. Zoals alle verbindingen van Sr, geeft dit zout een felrode kleur af in een vlam; in feite wordt het gebruikt als een bron van roodheid bij vuurwerk. De chemische eigenschappen liggen tussen die van bariumchloride, die giftiger is, en calciumchloride.
Strontiumchloride is de voorloper van andere strontiumverbindingen, zoals geel strontiumchromaat, strontiumcarbonaat en strontiumsulfaat. Blootstelling van strontiumchloride aan het natriumzout van het gewenste anion (of afwisselend koolstofdioxidegas om het carbonaat te vormen) leidt tot precipitatie van het zout
-Strontiumchloride wordt vaak gebruikt als rode kleurstof in pyrotechniek. Het geeft de vlammen een veel intensere rode kleur dan de meeste andere alternatieven.
-Het wordt in kleine hoeveelheden gebruikt in de glasindustrie en de metallurgie.
-Het radioactieve isotoop strontium-89, dat wordt gebruikt voor de behandeling van botkanker, wordt gewoonlijk toegediend in de vorm van strontiumchloride.
-Zeewateraquaria hebben kleine hoeveelheden strontiumchloride nodig, dat wordt verbruikt bij de aanmaak van de exoskeletten van bepaald plankton.
-Tandheelkunde
SrCl2 is nuttig bij het verminderen van tandgevoeligheid door een barrière te vormen over microscopisch kleine tubuli in het dentine die zenuwuiteinden bevatten die zijn blootgesteld door tandvleesontsteking. Bekend in de Verenigde Staten als Elecol en Sensodyne, worden deze producten "strontiumchloridetandpasta's" genoemd, hoewel de meeste tegenwoordig kaliumnitraat gebruiken, dat eerder werkt als een kalmerend middel dan als een barrière.
-Biologisch onderzoek
Korte blootstelling aan strontiumchloride induceert parthenogenetische activering van oöcyten die wordt gebruikt in ontwikkelingsbiologisch onderzoek.
-Ammoniumopslag
Een commercieel bedrijf gebruikt een op strontiumchloride gebaseerde kunstmatige vaste stof, AdAmmine genaamd, als een middel om ammonium onder lage druk op te slaan, voornamelijk voor gebruik bij NOx-emissiereductie op dieselvoertuigen. Ze beweren dat hun gepatenteerde materiaal ook van andere zouten kan worden gemaakt, maar ze hebben strontiumchloride gekozen voor massaproductie. Eerder onderzoek van het bedrijf overwoog ook het gebruik van het opgeslagen ammonium als een middel om synthetische ammoniumbrandstof op te slaan onder het handelsmerk HydrAmmine en de persnaam "waterstoftablet", maar dit aspect is niet gecommercialiseerd. Hun processen en materialen zijn gepatenteerd. Hun vroege experimenten gebruikten magnesiumchloride en worden ook genoemd in dat artikel