U heeft geen artikelen in uw winkelwagen
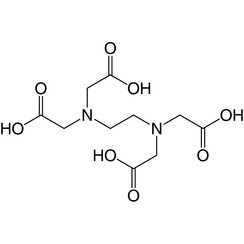
Ethyleendiaminetetraazijnzuur (EDTA)
Ethyleendiaminetetraazijnzuur (EDTA), ook bekend onder verschillende andere namen, is een chemische stof die wordt gebruikt voor zowel industriële als medische doeleinden. Het werd in 1935 voor het eerst gesynthetiseerd door Ferdinand Münz.
Het is een aminopolycarbonzuur en een kleurloze, in water oplosbare vaste stof. De geconjugeerde basis is ethyleendiaminetetraacetaat. Het wordt veel gebruikt om kalkaanslag op te lossen. Het nut ervan komt voort uit zijn rol als hexadentaat ("zestandige") ligand en chelaatvormer, d.w.z. zijn vermogen om metaalionen zoals Ca2 + en Fe3 + vast te leggen. Na door EDTA in een metaalcomplex te zijn gebonden, blijven metaalionen in oplossing maar vertonen een verminderde reactiviteit. EDTA wordt geproduceerd als verschillende zouten, met name dinatrium EDTA, calcium dinatrium EDTA en tetranatrium EDTA (typisch als hydraat).
Toepassingen
-Industrie
In de industrie wordt EDTA voornamelijk gebruikt om metaalionen in waterige oplossing op te slaan. In de textielindustrie voorkomt het dat metaalionverontreinigingen de kleuren van geverfde producten wijzigen. In de pulp- en papierindustrie remt EDTA het vermogen van metaalionen, vooral Mn2 +, om de disproportionering van waterstofperoxide, dat wordt gebruikt bij chloorvrij bleken, te katalyseren. Op een vergelijkbare manier wordt EDTA als conserveermiddel of stabilisator aan sommige voedingsmiddelen toegevoegd om katalytische oxidatieve verkleuring te voorkomen, die wordt gekatalyseerd door metaalionen. In frisdranken die ascorbinezuur en natriumbenzoaat bevatten, vermindert EDTA de vorming van benzeen (een carcinogeen).
De vermindering van de waterhardheid bij wastoepassingen en het oplossen van kalkaanslag in ketels vertrouwen beide op EDTA en aanverwante complexanten om Ca2 +, Mg2 + en andere metaalionen te binden. Eenmaal gebonden aan EDTA, hebben deze metalen centra de neiging geen neerslag te vormen of de werking van de zepen en wasmiddelen te verstoren. Om soortgelijke redenen bevatten schoonmaakoplossingen vaak EDTA. Op een vergelijkbare manier wordt EDTA gebruikt in de cementindustrie voor de bepaling van vrije kalk en vrije magnesiumoxide in cement en klinkers.
De oplosbaarheid van Fe3 + -ionen bij of onder een bijna neutrale pH kan worden bereikt met EDTA. Deze eigenschap is nuttig in de landbouw, inclusief hydrocultuur. Gezien de pH-afhankelijkheid van ligandvorming is EDTA echter niet nuttig voor het verbeteren van de ijzeroplosbaarheid in boven neutrale bodems. Anders vormt ijzer (III) bij bijna neutrale pH en hoger onoplosbare zouten, die minder biologisch beschikbaar zijn voor gevoelige plantensoorten. Waterig [Fe (EDTA)] - wordt gebruikt voor het verwijderen ("schrobben") van waterstofsulfide uit gasstromen. Deze omzetting wordt bereikt door het waterstofsulfide te oxideren tot elementaire zwavel, die niet-vluchtig is:
2 [Fe (EDTA)] - + H2S → 2 [Fe (EDTA)] 2− + S + 2 H +
In deze toepassing wordt het ijzer (III) -centrum gereduceerd tot zijn ijzer (II) -derivaat, dat vervolgens opnieuw door de lucht kan worden geoxideerd. Op vergelijkbare wijze worden stikstofoxiden uit gasstromen verwijderd met [Fe (edta)] 2−. De oxiderende eigenschappen van [Fe (edta)] - worden ook benut in fotografie, waar het wordt gebruikt om zilverdeeltjes op te lossen.
EDTA werd gebruikt bij de scheiding van de lanthanide-metalen door middel van ionenuitwisselingschromatografie. Geperfectioneerd door F. H. Spedding et al. in 1954, berust de methode op de gestage toename in stabiliteitsconstante van de lanthanide EDTA-complexen met atoomnummer. Met behulp van gesulfoneerde polystyreenparels en Cu2 + als een vasthoudend ion, zorgt EDTA ervoor dat de lanthaniden langs de harskolom migreren terwijl ze zich scheiden in banden van zuivere lanthaniden. De lanthaniden elueren in volgorde van afnemend atoomnummer. Vanwege de kosten van deze methode, in vergelijking met extractie met tegenstroom, wordt ionenuitwisseling nu alleen gebruikt om de hoogste zuiverheid van lanthaniden te verkrijgen (typisch meer dan 99,99%).
-Geneesmiddel
Een specifiek zout van EDTA, bekend als natriumcalciumedetaat, wordt gebruikt om metaalionen te binden in de praktijk van chelatietherapie, zoals voor de behandeling van kwik en loodvergiftiging. Het wordt op een vergelijkbare manier gebruikt om overtollig ijzer uit het lichaam te verwijderen. Deze therapie wordt gebruikt om de complicatie van herhaalde bloedtransfusies te behandelen, zoals zou worden toegepast om thalassemie te behandelen.
Tandartsen en endodontisten gebruiken EDTA-oplossingen om anorganisch vuil (smeerlaag) te verwijderen en de wortelkanalen in de endodontie te smeren. Deze procedure helpt bij het voorbereiden van wortelkanalen voor obturatie. Bovendien maken EDTA-oplossingen met de toevoeging van een oppervlakteactieve stof de verkalking in een wortelkanaal los en maken instrumentatie mogelijk (kanaalvorming) en vergemakkelijken de apicale voortgang van een bestand in een strak of verkalkt wortelkanaal naar de top.
Het dient als conserveermiddel (meestal om de werking van een ander conserveermiddel zoals benzalkoniumchloride of thiomersal te versterken) in oogpreparaten en oogdruppels.
Bij de evaluatie van de nierfunctie wordt het chroom (III) -complex [Cr (edta)] - (als radioactief chroom-51 (51Cr)) intraveneus toegediend en wordt de filtratie ervan in de urine gecontroleerd. Deze methode is nuttig voor het evalueren van de glomerulaire filtratiesnelheid (GFR) in de nucleaire geneeskunde.
EDTA wordt veel gebruikt bij de analyse van bloed. Het is een anticoagulans voor bloedmonsters voor CBC / FBE's, waarbij de EDTA het calcium in het bloedmonster cheleert, het coagulatieproces stopt en de morfologie van de bloedcellen in stand houdt. Buizen met EDTA zijn gemarkeerd met lavendel of roze toppen. EDTA is ook in tan top buizen voor het testen van lood en kan worden gebruikt in koningsblauwe top buizen voor het testen van sporenmetalen.
EDTA is een slijmdispergeermiddel en is zeer effectief gebleken bij het verminderen van bacteriegroei tijdens implantatie van intraoculaire lenzen (IOL's).
-Alternatief medicijn
Sommige alternatieve beoefenaars zijn van mening dat EDTA werkt als een antioxidant en voorkomt dat vrije radicalen de wanden van bloedvaten beschadigen, waardoor atherosclerose wordt verminderd. Deze ideeën worden niet ondersteund door wetenschappelijke studies en lijken in tegenspraak te zijn met enkele momenteel aanvaarde principes. De Amerikaanse FDA heeft het niet goedgekeurd voor de behandeling van atherosclerose.
-Cosmetica
In shampoos, reinigingsmiddelen en andere producten voor persoonlijke verzorging worden EDTA-zouten gebruikt als sekwestreermiddel om hun stabiliteit in de lucht te verbeteren.
-Laboratoriumtoepassingen
In het laboratorium wordt EDTA veel gebruikt voor het wegvangen van metaalionen: in de biochemie en moleculaire biologie wordt ionenuitputting vaak gebruikt om metaalafhankelijke enzymen te deactiveren, hetzij als een test voor hun reactiviteit of om schade aan DNA, eiwitten en polysacchariden te onderdrukken. EDTA fungeert ook als een selectieve remmer tegen dNTP-hydrolyserende enzymen (Taq-polymerase, dUTPase, MutT), leverarginase en mierikswortelperoxidase onafhankelijk van chelatie van metaalionen. Deze bevindingen dringen aan op de heroverweging van het gebruik van EDTA als biochemisch inactieve metaalionenvanger in enzymatische experimenten. In de analytische chemie wordt EDTA gebruikt bij complexometrische titraties en analyse van de waterhardheid of als maskeermiddel om metaalionen te isoleren die de analyses zouden verstoren.
EDTA vindt veel gespecialiseerde toepassingen in de biomedische laboratoria, zoals in de veterinaire oogheelkunde als anticollagenase om de verergering van hoornvlieszweren bij dieren te voorkomen. In weefselkweek wordt EDTA gebruikt als een chelaatvormer die aan calcium bindt en de verbinding van cadherines tussen cellen voorkomt, klontering van in vloeibare suspensie gekweekte cellen voorkomt of hechtende cellen losmaakt om te passeren. In de histopathologie kan EDTA worden gebruikt als ontkalkingsmiddel, waardoor het mogelijk is om coupes te snijden met een microtoom zodra het weefselmonster is gedemineraliseerd. Van EDTA is ook bekend dat het een reeks metallopeptidasen remt, de remmingsmethode vindt plaats via de chelatie van het metaalion dat nodig is voor katalytische activiteit. EDTA kan ook worden gebruikt om te testen op biologische beschikbaarheid van zware metalen in sedimenten. Het kan echter de biologische beschikbaarheid van metalen in oplossing beïnvloeden, wat tot bezorgdheid kan leiden over de effecten ervan op het milieu, vooral gezien het wijdverbreide gebruik en toepassingen.